科技日报记者 付丽丽
长期社交隔离不仅影响情绪,还可能在大脑中触发特定分子通路,诱发焦虑。近日,华南理工大学、浙江大学等团队在《细胞·代谢》发表研究,首次提出“铁可塑性”(ferroplasticity)概念,揭示社交隔离如何通过腹侧海马(vHip)神经元驱动焦虑。
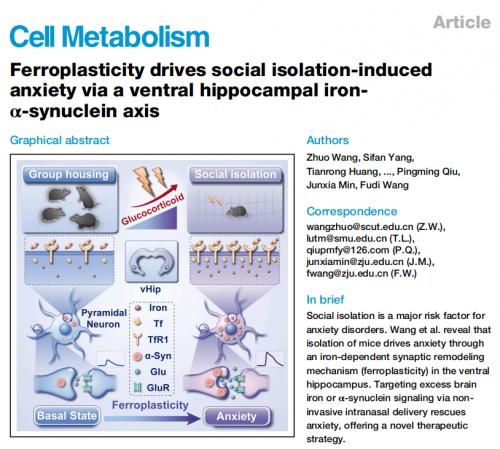
研究发现,社交隔离使小鼠应激激素升高,特异性激活vHip锥体神经元中的糖皮质激素受体(GR)。GR通过诱导转录因子c-Jun,上调转铁蛋白受体1(TfR1),导致神经元内铁异常蓄积。这种铁积累不引起细胞死亡,而是解除铁调节蛋白对α-突触核蛋白(α-Syn)mRNA的抑制,促使其大量合成。
传统上与帕金森病相关的α-Syn,在此扮演“突触放大器”:增强谷氨酸释放、增加树突棘密度,导致vHip神经元超兴奋,引发焦虑样行为。敲除α-Syn或抑制其表达可有效阻断焦虑,而不影响上游铁积累,证实其为关键效应分子。
基于该通路,团队开发出两种鼻腔给药策略:美国食品药品监督管理局(FDA)批准的铁螯合剂去铁胺(DFO)和靶向α-Syn的反义寡核苷酸(ASOs)。在治疗模型中,二者均能在两周内显著缓解已形成的焦虑,效果优于自然恢复。
业内专家表示,该研究首次将社会心理应激、脑铁代谢与突触可塑性联系起来,提出“铁可塑性”这一可干预的生物学机制,为焦虑障碍提供了全新治疗思路。孤独不再只是情感体验,更是一种可被精准调控的神经病理状态。




 网友评论
网友评论















