科技日报记者 王春 通讯员 殷梦昊 邓晗
肿瘤免疫治疗药物未来可能可以口服了?复旦大学的最新研究成果为此提供了潜在的技术基础。3月19日晚,复旦大学鲁伯埙团队联合粤港澳大湾区精准医学研究院宋海坤团队、海军军医大学盛春泉团队,在国际顶尖学术期刊《细胞》在线发表重磅研究,开创性地建立全新靶向蛋白降解策略ERADEC,突破现有技术瓶颈,有望让肿瘤免疫治疗迈入“口服时代”,为跨膜蛋白相关疾病药物研发开辟全新路径。
蛋白靶向降解技术是小分子药物领域的研究热点,其核心优势是能选择性清除致病蛋白,从根源上解决疾病问题。但目前主流技术如PROTAC等,对大多数跨膜蛋白“束手无策”;即便近年出现的LYTAC、GlueTAC等改进技术,也多依赖生物大分子修饰,不仅无法实现口服,成本偏高,降解效率还受细胞内途径限制,成为行业亟待突破的痛点。
针对这一难题,鲁伯埙团队另辟蹊径,将目光投向细胞内未被充分开发的内质网相关降解(ERAD)途径。“ERAD本是细胞清除折叠异常蛋白的‘质检员’,我们大胆设想,能否‘劫持’这一系统,让它精准降解致病跨膜蛋白。”鲁伯埙介绍,这一构想的关键,是找到能触发ERAD系统的小分子。
机缘巧合之下,团队在前期亨廷顿病致病蛋白降解研究中获得突破——发现小分子化合物desonide可直接结合内质网E3泛素连接酶SYVN1,进而促进致病蛋白降解。基于这一发现,团队提出ERADEC(ERAD-engaging chimera)原创构想,设计出兼具“识别”与“连接”功能的小分子化合物:一端绑定SYVN1,另一端精准识别靶蛋白,通过化学连接子形成三元复合物,最终触发靶蛋白泛素化并被ERAD系统降解。
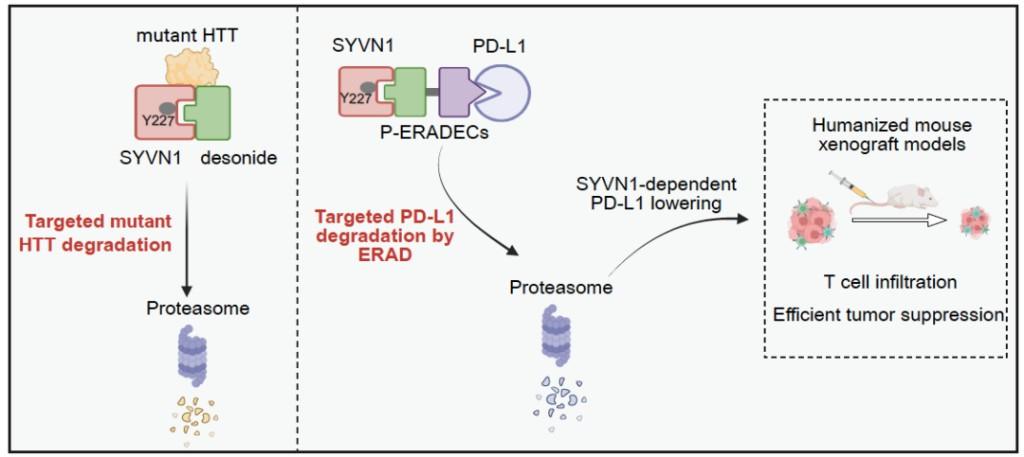

为验证这一策略的有效性,团队以肿瘤免疫治疗关键靶点PD-L1蛋白为模型展开实验。结果令人振奋:ERADEC能显著降低细胞内PD-L1蛋白水平,且这一过程严格依赖SYVN1及ERAD通路;在人免疫细胞重构的小鼠肿瘤模型中,其抗肿瘤效果甚至优于目前临床广泛应用的PD-L1抗体药物。
更具里程碑意义的是,ERADEC展现出强大的平台化潜力。“通过更换目标配体,我们成功实现了对多种跨膜蛋白的降解。”鲁伯埙表示,这意味着该技术可拓展至肿瘤、代谢性疾病、神经退行性疾病等多个领域,为长期难以干预的跨膜蛋白靶点提供了全新降解方案。
这项成果的诞生,离不开近十年的精耕细作,更源于一次意外发现。团队曾在筛选亨廷顿病致病蛋白降解分子时,找到有效小分子却始终无法明确其作用机制。鲁伯埙带领团队深耕一年多,最终锁定内质网E3连接酶,这也成为ERADEC技术的核心起点。2024年,该设想得到ERAD领域国际权威专家的肯定与鼓励,更坚定了团队深耕这一方向的决心,为后续成果落地奠定了坚实基础。
研究中,AI for Science理念发挥了重要作用。团队借助大模型预测蛋白三维结构及小分子与蛋白的结合模式,为分子改造提供了关键支撑。目前,团队已通过药物化学改造,获得具有一定口服利用度的ERADEC分子,未来有望开发出口服肿瘤免疫药物,替代传统静脉注射抗体药物,大幅降低治疗成本,提升患者生活质量。
与传统抗体药相比,ERADEC小分子降解剂优势突出:无需饱和结合靶蛋白,皮摩尔到纳摩尔量级即可起效,能彻底降解靶蛋白,且小分子可循环利用,作用更彻底、副作用更小。据悉,目前,论文相关专利已与药企签署许可协议,团队正加快推进第二代小分子药物研发,推动基础研究成果早日落地,惠及更多患者。




 网友评论
网友评论















