科技日报记者 韩荣
3月23日,记者从山西医科大学获悉,该校张承武、陆利、刘文团队联合吕梁学院刘涛,研发出一款针对帕金森病的新型近红外荧光探针,还构建了兼具监测与干预功能的纳米平台,为帕金森病的精准诊疗开辟了全新路径。相关成果发表在《先进科学》。
帕金森病作为全球第二大神经退行性疾病,给患者和家属带来了沉重的负担。这种疾病的病理进程十分隐匿,往往当手抖、行动迟缓等临床症状显现时,患者大脑内的多巴胺能神经元已发生不可逆损伤,这也让帕金森病的早期发现和有效干预成为医学领域的一大难题。
山西医科大学基础医学院教授张承武介绍,铁死亡是一种依赖铁、非凋亡型的程序性细胞死亡模式,近年来发现其与帕金森病的发生和发展密切相关。在这一过程中,会出现两大核心特征,细胞内亚铁离子的异常堆积,以及细胞内黏度的明显升高,这两个指标的变化成为监测帕金森病相关铁死亡的关键信号。但此前的荧光探针只能靶向单一生物标志物,在复杂的人体生理环境中,容易出现特异性不足、监测不准确的问题,难以满足帕金森病精准诊断的需求。
针对这一痛点,团队通过分子工程技术合成出一系列新型近红外荧光探针。这款探针的“聪明”之处在于,它并非单一识别某个信号,而是只有在亚铁离子和黏度同时升高时,才会被“点亮”发出荧光信号,从根本上突破了传统探针的局限。
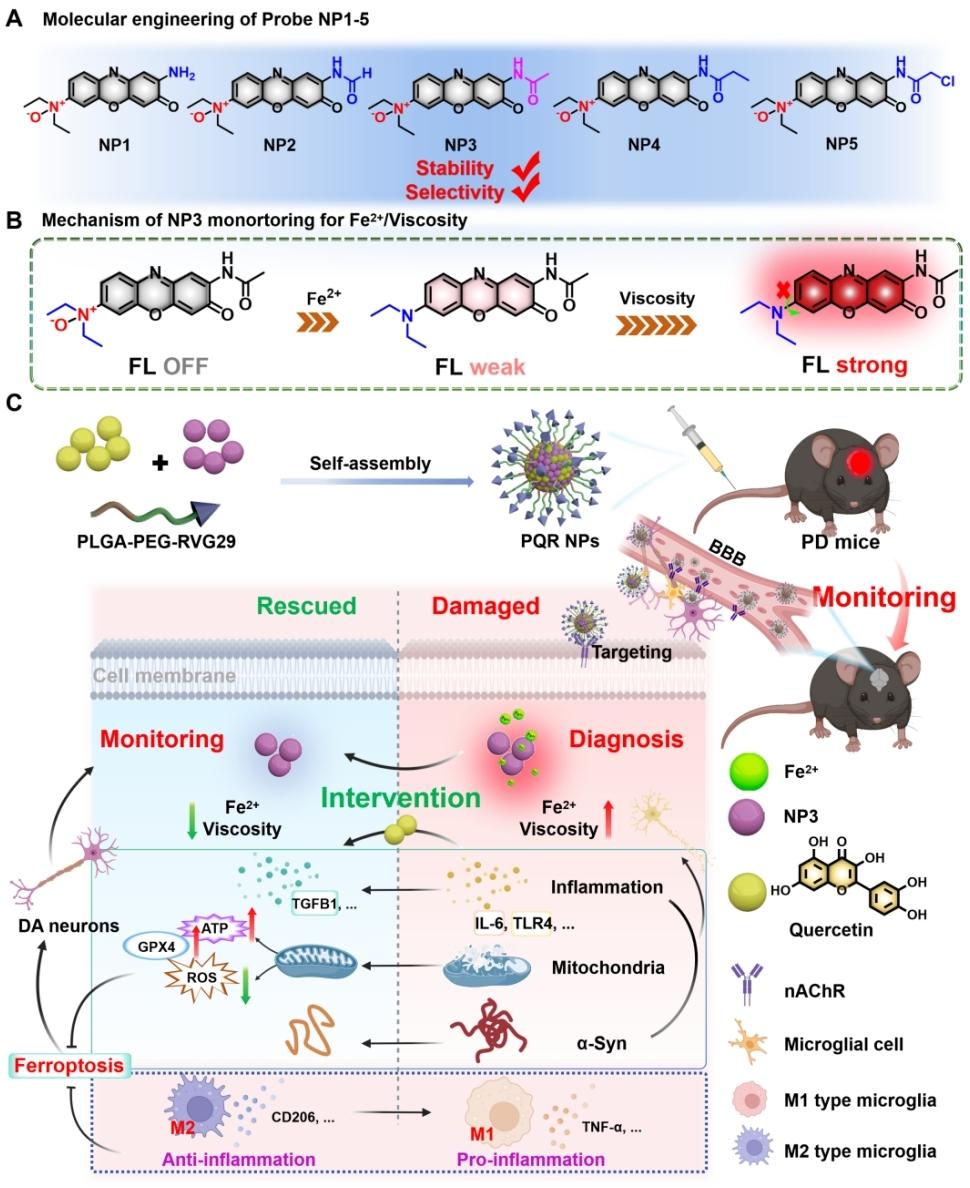
经过实验验证,其中的NP3近红外荧光探针表现尤为突出,不仅拥有高灵敏度、高选择性,还具备良好的生物相容性,在细胞、果蝇、秀丽隐杆线虫等多种帕金森病模型中,都能清晰、准确地捕捉到铁死亡过程中亚铁离子和黏度的细微变化,就像为科研人员和医生装上了一双“透视眼”,能实时观察帕金森病相关的病理变化。
仅仅实现精准监测还不够,张承武表示,团队还从“诊断”与“干预”结合的方式入手,打造一体化的诊疗方案。为此,研究人员以NP3近红外荧光探针为监测核心,搭配了天然活性化合物槲皮素。这种物质拥有抑制铁死亡、抗炎、抗氧化的多重功效,是干预帕金森病进展的“好帮手”,但它水溶性差、生物利用度低,还难以穿过血脑屏障到达病变部位,临床应用受限。
团队将两者结合,构建出新型纳米平台PQR NPs,成功解决了槲皮素的应用难题,同时让这个纳米平台兼具了双重功能。一方面,它能依靠NP3近红外荧光探针持续监测帕金森病模型中铁死亡相关的亚铁离子和黏度变化,为疾病诊断和干预效果评估提供直观、实时的依据;另一方面,平台搭载的槲皮素能通过多种途径发挥作用,抑制铁死亡、减轻脑部炎症、保护多巴胺能神经元,有效干预帕金森病的进展。
这一研究成果实现了帕金森病“诊断—干预—监测”的有机融合,不仅为深入理解帕金森病中铁死亡的发病机制提供了强有力的工具,也为帕金森病这类神经退行性疾病的精准诊疗提供了全新的纳米医学策略。




 网友评论
网友评论