科技日报记者 雍黎 通讯员 李荣荣
5月10日,记者从陆军军医大学新桥医院获悉,该院医院检验医学中心李忠俊教授团队的一项研究成果近日登上国际顶级血液学期刊《血液》,阐明了Ⅱ型遗传性血小板减少症的发病新机制,这不仅为该罕见遗传性血液病的精准治疗及药物研发提供了全新靶点和思路,更为血小板再生提供了新的策略。

Ⅱ型遗传性血小板减少症是一种遗传性血液病,患者因血液中血小板持续低下,终身面临出血风险,并有10%的风险发展为血液肿瘤。自2011年发现其致病基因以来,一个矛盾现象始终无法解释:患者骨髓中负责生产血小板的“母细胞”数量并不少,但外周血中的血小板就是不够用。
“这就像一个工厂里的工人数量充足,但就是产不出产品,原因困扰了我们15年。”李忠俊表示。为揭开谜底,其团队联合国内外专家,利用先进的单细胞组学等技术,对数万个人体细胞进行了精准追踪。
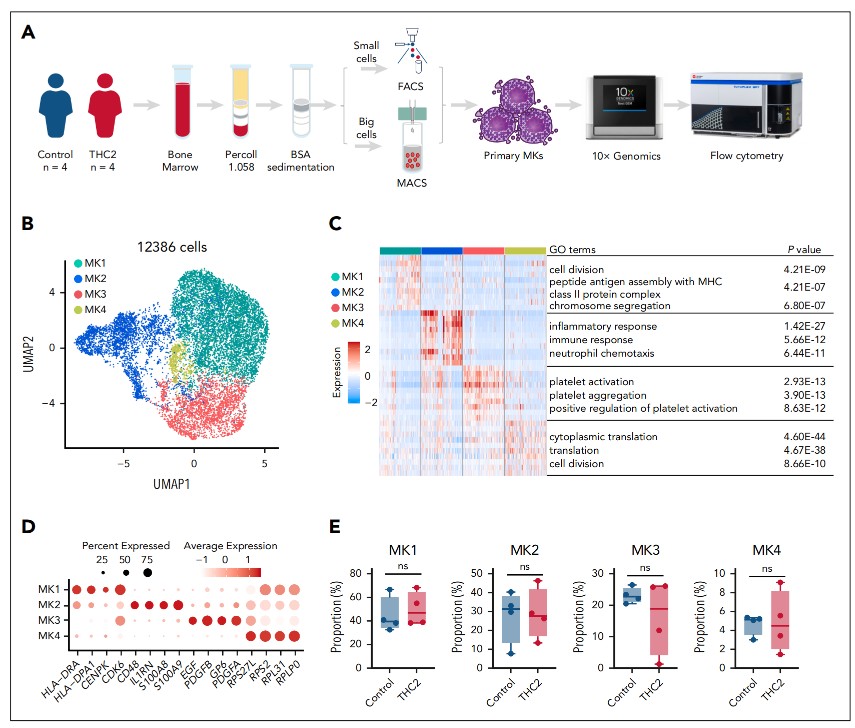
研究最终发现,致病的ANKRD26蛋白竟是一个“双面角色”。在疾病早期,它像“生长燃料”,刺激骨髓中的“母细胞”增多;但在细胞发育后期准备“生产”血小板的关键时刻,它却“变身”为“毁灭者”,激活一条全新的JUNB-p21自杀信号通路,导致大量本应“分娩”血小板的成熟细胞“程序性死亡”。
“正是这种‘先促增、后诱杀’的矛盾机制,导致了‘母细胞多、血小板少’的临床悖论。”科研人员表示。该发现不仅完美解释了长期悬而未决的科学疑问,更重要的是,首次揭示的JUNB-p21通路为未来开发靶向治疗药物提供了明确的“靶标”。
对于这项研发成果,《血液》专门配发评论文章,高度评价此项研究“成功破解了困扰医学界15年的临床悖论”。这意味着,未来患者有望通过针对性药物,阻断这一错误“自杀程序”,从而从根源上提升血小板数量。该研究不仅为该罕见病的患者带来精准治疗的新希望,也为促进血小板再生与提高人造血小板效率提供了新的策略。
(受访者供图)




 网友评论
网友评论