科技日报记者 刘园园
记者3月18日从西湖大学获悉,该校申恩志团队的研究成果首次揭示一种比基因小得多的分子——小RNA是决定生命能否成功启动的关键。这为科学界理解生命诞生之初的精密调控提供了全新视角。
作为一种非常重要的生殖细胞,卵母细胞内部高度富集着一类小RNA分子(内源性siRNA),后者被证实与早期胚胎发育密切相关。siRNA的核心功能,是精准识别并“剪断”特定的RNA,从而抑制对应蛋白质的表达。“只有真正看清它们在卵母细胞中‘剪切’了什么,才能理解它们为何对生命起始如此重要。”申恩志说。
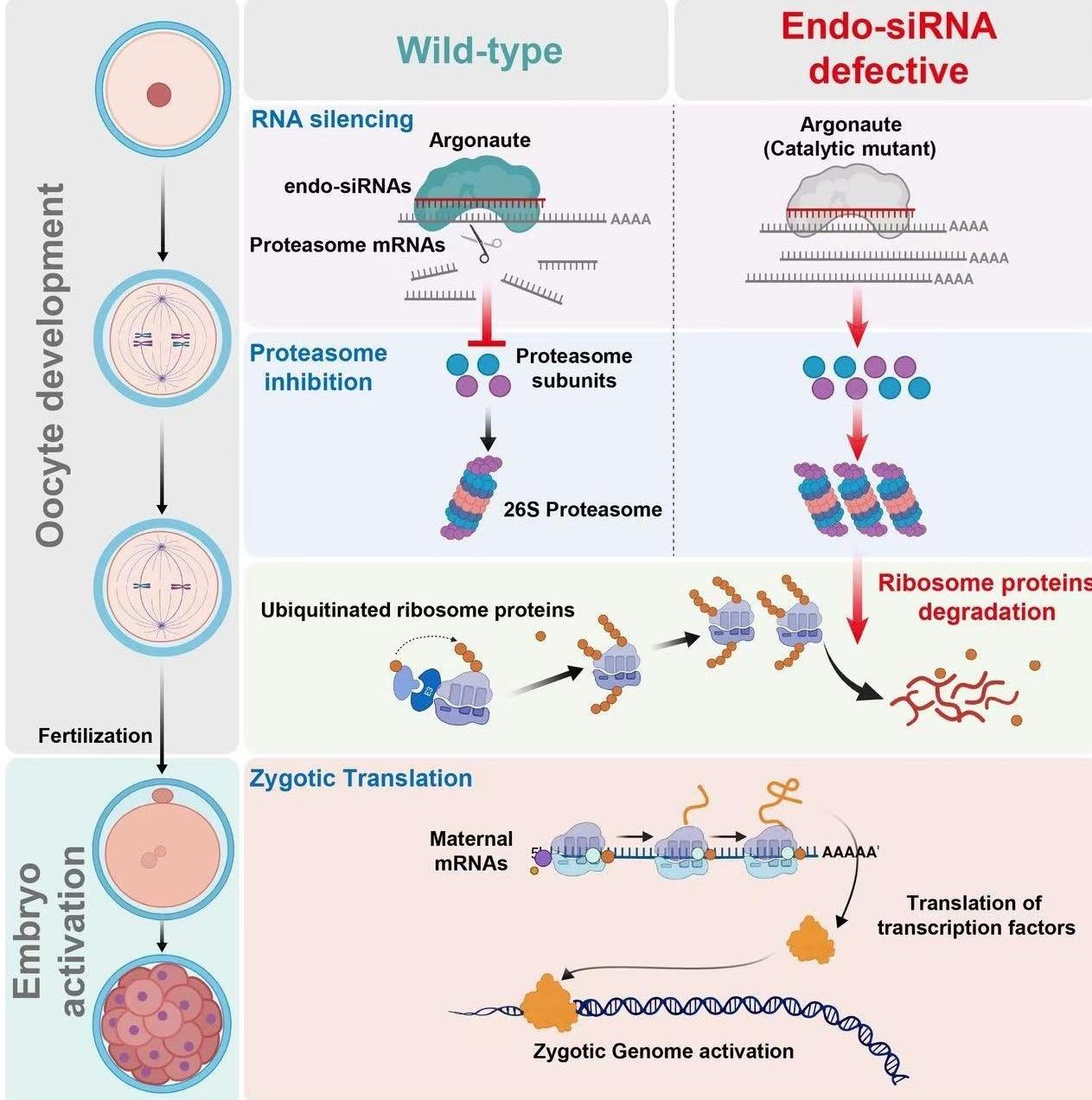
申恩志团队对小RNA切割文库构建技术(CLASH技术)进行了系统性改进,并使其适配卵母细胞样本。他们历经近3年攻关,首次绘制出小鼠卵母细胞内源性 siRNA的靶向切割图谱。
研究发现,siRNA的剪切目标是细胞里的“粉碎机”——蛋白酶体。siRNA在特定蛋白的辅助下,精准切割蛋白酶体关键转录本,抑制其活性,避免核糖体被过度降解,从而保障胚胎早期发育。也就是说,小RNA并不直接推动生命前进,而是通过抑制“破坏力”,保护“创造力”,为生命按下真正的“启动键”。
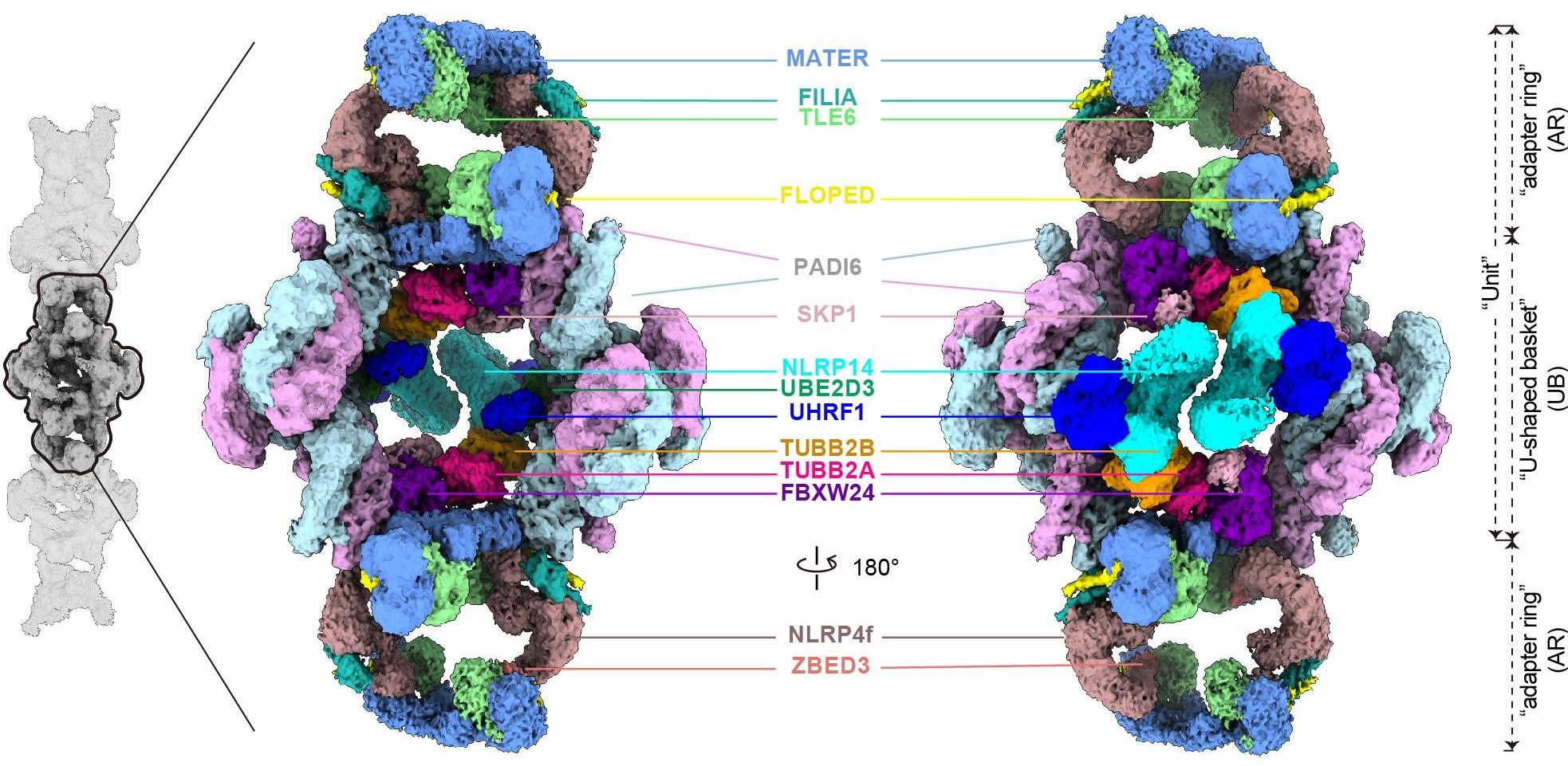
此外,卵母细胞中占细胞质体积近10%的细胞质晶格(CPL),其组成和结构此前也一直是未解之谜。在另一项研究中,申恩志团队利用冷冻电镜技术,成功解析了其原子级结构。研究发现,细胞质晶格由14种蛋白质精密组装而成,并以特定结构交替排列形成纤维骨架,是高度有序的超级分子结构。
这些研究成果为理解女性不孕、反复胚胎停育等临床问题提供了全新视角。“一些女性面临不孕、反复流产或胚胎停育的问题,往往找不到原因。现在我们知道,如果卵母细胞中的小RNA通路出了问题,或者细胞质晶格结构不稳定,就可能导致胚胎在最早期发育失败。”申恩志表示,未来,医生或许可以通过检测这些分子标志物,提前预警风险,优化辅助生殖技术的成功率。
(西湖大学供图)




 网友评论
网友评论