科技日报记者 张佳星
“我们自主研发的肿瘤类器官试剂盒刚刚与医疗大模型、手术机器人一并纳入了创新医疗器械特别审查程序。”5月10日,北京大学未来技术学院教授、北京基石医学检验实验室有限公司创始人席建忠告诉科技日报记者,这是首个肿瘤类器官产品获得国家药品监督管理局的“创新医疗器械特别审查程序”审评许可,将助力具有自主知识产权的肿瘤细胞体外培养技术尽快落地临床,为肿瘤患者高效精准地找到更优诊疗方案。
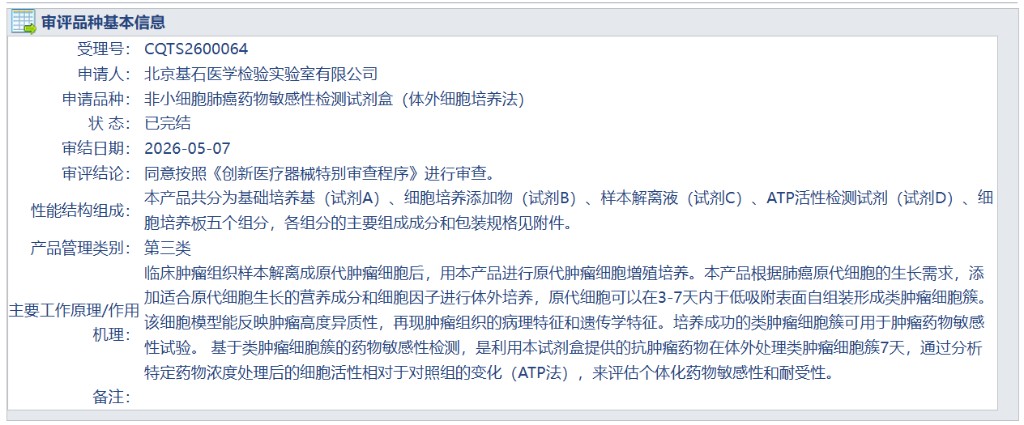
据介绍,通过独特的细胞培养技术形成体外模型、为肿瘤患者制定个体化用药方案,正在成为解决临床精准用药痛点的前沿趋势。近年来,国内外在肿瘤类器官测试方面开展了大量的研究,但实现临床可用的仍是少数。
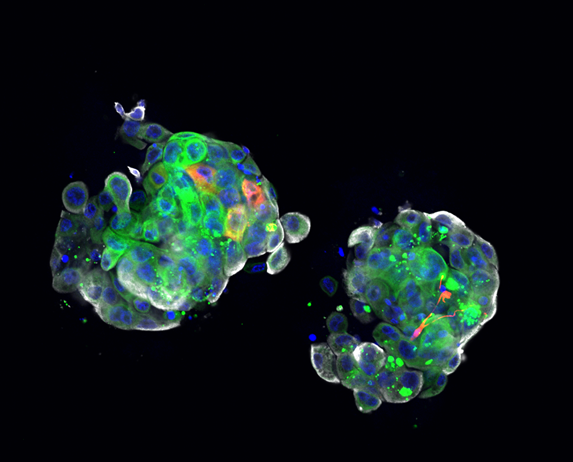
“有别于目前应用广泛的基因检测,肿瘤类器官技术通过直接从患者肿瘤组织中分离原代细胞进行培养,目的是在体外‘模拟’患者肿瘤,然后测试药物。”席建忠告诉记者,构建与患者肿瘤生物学特征高度一致的体外药敏模型需要攻克很多核心技术,同时为了能够将技术转化为可用的产品,还要满足临床要求,不能太贵也不能让患者等得太久,因此在技术转化时要不断打磨,控制成本、缩短试验周期。
为此,团队自主研发了自组装微肿瘤(PTC)原代肿瘤细胞体外培养平台,采用悬浮体系3D培养方式,赋予培养细胞自组装能力,高度还原肿瘤微环境特征。相较于其他肿瘤类器官技术,自组装微肿瘤的测试成本更低,测试周期大幅缩减至不到14天。
“我们与上海市胸科医院、北京大学肿瘤医院等单位合作对产品进行了测试,结果显示产品预测抗肿瘤药物疗效的准确率达到89%。”席建忠说,产品解决了传统类器官标准化生产及药效检测分析难点,其操作简便、无经验人员也能在48小时内完成培训并独立操作的优势更是得到医疗机构认可。未来,在特别审查程序的支持下,国家药品监督管理局将直接指导团队开展临床试验,避免临床试验设计不合理等问题的出现,提高临床研究效率,促进创新产品快速惠及患者。
(受访者供图)




 网友评论
网友评论