科技日报记者 刘霞
据最新一期《自然·生物医学工程》论文,美国加州大学伯克利分校团队利用微型器官芯片系统加速了人体脂肪与肝脏组织生物年龄,在短短4天内,以高度生理学准确性模拟了源于诱导多能干细胞的组织约40年的衰老过程。这项新技术可帮助人们更便捷地理解衰老机制,并筛选抗衰老疗法,而无需等待数年才能获得结果。
这款器官芯片模拟了人体“肝脂交互网络”。芯片内,源自人类诱导多能干细胞的脂肪与肝细胞,被置于独立却相通的腔室。微流控通道模拟血液循环,使营养液在组织间流动,重建器官间的“对话”。
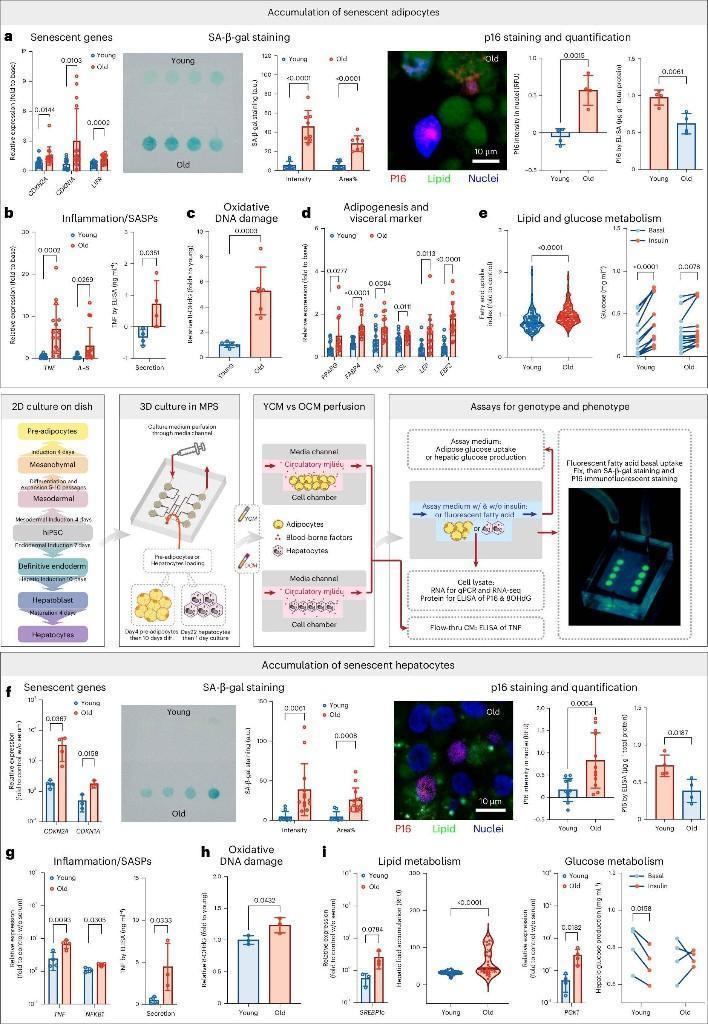
团队将新生组织浸润于62岁以上捐赠者的血清中循环,并以21—34岁年轻捐赠者血清作为对照。结果显示,器官芯片中接触老年血清的细胞,在4天内便呈现出需数十年才能在人体出现的慢性炎症、血糖调节受损及脂肪代谢紊乱。
此外,传统观点认为,损伤积累是随机的漫长过程,但最新研究显示,损伤时刻发生,细胞亦在时刻修复。衰老血清似乎抑制了修复能力,加速了损伤堆积。
研究还揭示了衰老的“传染性”与性别差异。当衰老的脂肪组织与年轻肝脏相连,肝细胞亦会染上衰老迹象。而尽管干细胞基因相同,但男性血清处理的脂肪组织炎症更重、衰老更甚,印证了男性衰老更快、寿命更短的认知。
该研究同时利用器官芯片评估了抗衰老疗法,测试了包括雷帕霉素、催产素等多种干预手段。结果显示,催产素在减少炎症、延缓衰老及提高胰岛素敏感性方面表现卓越,而雷帕霉素在此实验中效果甚微。
除作为测试平台外,团队还锁定了11种此前未被关联的新型衰老生物标志物,为药物开发提供了新靶点。目前,该技术已申请专利,商业化进程正在加速。




 网友评论
网友评论